มีคนจำนวนนับพันที่ต้องการผ่าตัดเปลี่ยนหัวใจ ซึ่งนี่เองที่ทำให้นักวิจัยพยายามเพาะเลี้ยงหัวใจขึ้นมาให้ได้
วิดีโอแสดงวิธีการเพาะเลี้ยงหัวใจ: Harald Ott และคณะได้ทดสอบความทนทานของส่วนต่างๆ ของหัวใจสร้างขึ้นมา
ดอริส เทเลอร์ (Doris Taylor) เธอไม่ได้รู้สึกเลยว่าเธอเองถูกต่อว่าเมื่อใครๆ รอบๆ ตัวเธอต่างก็เรียกเธอเรียกว่า ดร.แฟรงเกนสไตน์ “จริงๆ แล้ว ฉันถือว่ามันเป็นคำชมที่ยิ่งใหญ่มากที่ฉันเคยได้รับมากต่างหาก” ซึ่งยืนยันจากงานวิจัยของเธอที่ได้เพิ่มขอบเขตของคำว่า “เป็นไปได้” จากงานที่เธอเป็นนักวิจัยด้านเวชศาสตร์ฟื้นฟูที่ สถาบันหัวในเทกซัส เธอยอมรับว่าการเปรียบเทียบเธอกับ ดร.แฟรงเกนสไตน์ เป็นเรื่องที่เหมาะสมแล้ว เพราะว่าปกติแล้ว เธอจะเก็บเอาอวัยวะ อาทิ หัวใจ และปอด จากผู้เสียชีวิตใหม่ๆ และจัดการสิ่งเหล่านั้นตั้งแต่ระดับเซลล์เพื่อที่จะพยายามที่จะทำให้อวัยวะชิ้นนั้นๆ กลับมามีชีวิตได้อีกครั้ง โดยในใจก็หวังเพียงแค่ว่า หัวใจที่ตายไปแล้วจะเริ่มเต้นใหม่ หรือปอดจะหายใจได้ใหม่อีกครั้งหนึ่ง
เทเลอร์ เป็นนักวิจัยแนวหน้าที่อยากจะสร้างอวัยวะใหม่ขึ้นมาทั้งหมด และอยากให้การปลูกถ่ายอวัยวะชิ้นนั้นๆ ปราศจากความเสียงของการปฏิเสธอวัยวะจากระบบภูมิคุ้มกันของคนไข้เลย โดยเธอใช้หลักการง่ายๆ ซึ่งเริ่มจากการกำจัดเซลล์ดั้งเดิมทั้งหมดออกจากอวัยวะไปเสียก่อน โดยอวัยวะชิ้นนี้อาจจะได้มาจากมนุษย์หรือไม่ก็ได้ การกำจัดเซลล์ดั้งเดิมนี้จะทิ้งเอาโปรตีนที่เป็นโครงสร้างของอวัยวะชิ้นนั้นๆ ไว้ หลังจากนั้นก็จัดการเอาสเต็มเซลล์ ที่มีระบบภูมิคุ้มกันที่ตรงกับผู้ป่วยที่ต้องการอวัยวะนั้นๆ มาเลี้ยงบนโครงสร้างโปรตีน ซึ่งวิธีนี้ปัญหาของการต่อต้านอวัยวะของผู้ป่วยที่ต้องการปลูกถ่ายอวัยวะก็หมดไป
ในทางปฏิบัติแล้ว กระบวนการนี้เผชิญกับความท้าทายหลากหลายด้าน โดยปกติแล้วนักวิจัยสามารถเพาะเลี้ยง และปลูกถ่ายอวัยวะที่มีโพรงอยู่ตรงกลาง เช่นพวก หลอดลม และกระเพาะปัสสาวะได้สำเร็จ แต่ว่าการเพาะเลี้ยงอวัยวะตันๆ ที่มีเซลล์อยู่ทุกส่วนของอวัยวะ อาทิ ไต หรือปอด เป็นอวัยวะที่ต้องการเซลล์หลากหลายประเภท และเซลล์แต่ละประเภทจะต้องวางตัวอยู่ที่ตำแหน่งที่ถูกต้องเหมาะสม และนอกเหนือจากนั้นก็คือ อวัยวะเหล่านี้จะต้องมีการเพาะเลี้ยงเครือข่ายของหลอดเลือดที่สลับซับซ้อนไปด้วยพร้อมๆ กัน เพื่อทำให้อวัยวะชิ้นนั้นๆ มีชีวตขึ้นมาได้ อวัยวะประดิษฐ์ชิ้นใหม่นี้ จะต้องปราศจากจากเชื้อโรคใดๆ และต้องเจริญเติบโตไปตามอายุคนไข้ได้ สำหรับกรณีที่คนไข้ยังเด็กอยู่ หรืออย่างน้อยที่สุดก็ต้องสามารถที่จะซ่อมแซมตัวเอง และสิ่งที่สำคัญที่สุดก็คือ อวัยวะเหล่านั้นมันจะต้องทำงานได้จริง ตราบจนสิ้นอายุขัยของคนไข้ โดยหัวใจเป็นอวัยวะที่เป็นที่ต้องการเปลี่ยนถ่ายเป็นลำดับที่สาม รองจาก ไต และตับ ถ้านับจากจำนวนผู้ป่วยที่รอการเปลี่ยนถ่ายอวัยวะ เฉพาะในประเทศอเมริกา มีอยู่ประมาณ 3,500 ราย และการเปลี่ยนถ่ายหัวใจก็มีความท้าทายพิเศษมากมายรออยู่ กล่าวคือ หัวใจจำเป็นจะต้องเต้น เพื่อปั๊มเลือดอย่างต่อเนื่อง เป็นปริมาณ 7,000 ลิตร ต่อวัน โดยต้องไม่เสียหาย ห้องต่างๆ และลิ้นหัวใจต่างๆ ของหัวใจ ต้องสร้างจากเซลล์กล้ามเนื้อจำเพาะหลากหลายชนิดที่เรียกว่า “cardiomyocytes” และหัวใจสมบูรณ์ที่ได้รับการบริจาคนั้นหายากมาก เพราะว่าบ่อยครั้งที่หัวใจของผู้บริจาคจะเสียหายมาแล้ว ด้วยเนื่องจากอาการโรคต่างๆ ก่อนที่จะเสียชีวิต หรือไม่ก็ความเสียหายจากความพยายามกู้ชีวิตผู้บริจาคหัวใจ ดังนั้นหัวใจที่ได้จากวิศวกรรมเนื้อเยื่อจึงยังคงเป็นที่ต้องการอย่างสูง
เทเลอร์ เคยประสบความสำเร็จจากการทดลองสร้างหัวใจของหนูมาแล้ว [1] มองความท้าทายเรื่องนี้ว่า “มันจะต้องทำได้แน่นอน” และเธอก็กล่าวต่อไปอีกว่า “แต่มันคงจะไม่ใช่เรื่องง่ายๆ” แต่ Paolo Macchiarini ศัลยแพทย์ทรวงอก และนักวิทยาศาสตร์ ผู้ที่เคยทำการผ่าตัดปลูกถ่ายหลอดลมประดิษฐ์ให้กับผู้ป่วยหลายรายแล้ว กลับกล่าวว่า ถึงแม้ว่าการผ่าตัดปลูกถ่ายอวัยวะประดิษฐ์กำลังจะเป็นเรื่องปกติสำหรับอวัยวะที่เป็นท่อ อาทิ หลอดลม หลอดเลือด และหลอดอาหาร แต่เขายังคง “ไม่เชื่อมันว่าการผ่าตัดปลูกถ่ายอวัยวะประดิษฐ์จะเกิดขึ้นกับอวัยวะที่ซับซ้อนมากๆ ได้”
แต่อย่างไรเสียก็ตามความพยายามแบบนี้ยังคุ้มค่าเสมอ ถึงแม้ว่ามันจะล้มเหลวก็ตาม Alejandro Soto-Gutiérrez นักวิจัยและศัลยแพทย์แห่งมหาวิทยาลัยพิตส์เบิร์ก กล่าว “นอกเหนือจากความต้องการที่จะประดิษฐ์อวัยวะเพื่อการปลูกถ่ายแล้ว มันมีอะไรอีกมากมายที่เราจะได้เรียนรู้จากระบบนี้” อาทิ ความเข้าใจขั้นพื้นฐานที่ดีขึ้นเกี่ยวกับการจัดเรียงตัวของเซลล์ต่างๆ ในหัวใจ และการพิสูจน์แนวความคิดใหม่ๆ ของการแก้ไขปัญหาเรื้อรังในการปลูกถ่ายอวัยวะ
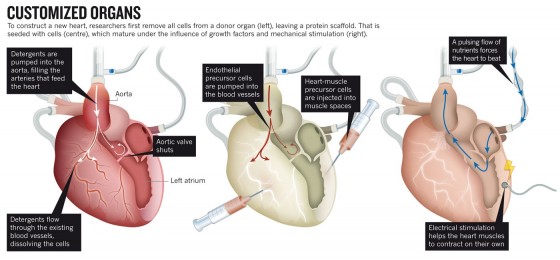
โครงสร้าง
กว่าทศวรรตแล้วที่นักวิจัยสามารถเปลี่ยนสเต็มเซลล์จากเอ็มบริโอ ให้กลายเป็นเซลล์หัวใจที่สามารถเต้นได้ในห้องปฏิบัติการ โดยการใช้อุปกรณ์ไฟฟ้ามากระตุ้นการเต้นของหัวใจจากภายนอก ทำให้เซลล์หัวใจเหล่านี้สามารถเต้นเป็นจังหวะได้ และสามารถรักษาจังหวะการเต้นให้ประสานกันได้นานหลายชั่วโมง
ก้อนเนื้อที่เต้นได้จากจานเพาะเลี้ยงเนื้อเยื่อ เอาไปพัฒนาไปเป็นหัวใจที่ทำงานได้จริงๆ ในโครงสร้างสามมิตินั้น นักวิจัยอาจจะใช้สร้างโครงสร้างของหัวใจแบบนี้ได้จากเครื่องพิมพ์สามมิติก็ได้ เช่นเดียวกับหลอดลมประดิษฐ์ที่ได้แสดงไว้ตั้งแต่เมื่อต้นปีนี้ [2] แต่อย่างไรก็ตาม อวัยวะที่ซับซ้อนอย่างเช่น หัวใจของมนุษย์นี้ อยู่เหนือกว่าเครื่องมือที่ซับซ้อนใดๆ บนโลกที่จะเลียนแบบได้ และหัวใจมนุษย์ก็จะยิ่งซับซ้อนมากขึ้นไปยิ่งขึ้นอีก เมื่อเรารวมเครื่อข่ายที่สลับซับซ้อนของเส้นเลือดฝอยของหัวใจ ที่มีหน้าที่นำเอาออกซิเจนและสารอาหารไปหล่อเลี้ยงหัวใจ และกำจัดของเสียออกมาจากเซลล์กลามเนื้อหัวใจ โดยเฉพาะอย่างยิ่งจากเนื้อเยื่อด้านในลึกๆ “ระบบหลอดเลือดในหัวใจ เป็นความท้าทายที่ยิ่งใหญ่ที่สุด” Anthony Atala แพทย์ผู้เชี่ยวชาญด้านปัสสาวะวิทยาผู้ที่เคยผ่าตัดเปลี่ยนถ่ายกระเพาะปัสสาะประดิษฐ์กล่าว [3] และเขายังคงทำงานสร้างไตอยู่
แต่ว่าเทคนิคพิเศษของการสร้างหัวใจก็คือ การนำของที่สิ่งมีชีวิตผลิตไว้แล้วนำกลับมาใช้ใหม่ สถานที่แห่งหนึ่งที่เหมาะสำหรับการดูว่ามันทำได้อย่างไร คือที่โรงพยาบาลกลางแมสสาซูเสตส์ ในบอสตัน โดย Harrald Ott ศัลยแพทย์ และนักวิจัยด้านเวชศาสตร์ฟื้นฟู ได้สาธิตวิธีที่เขาได้พัฒนา จากตอนที่เขาฝึกงานอยู่กับเทเลอร์ในช่วงปี 2000
หัวใจของผู้เสียชีวิตได้รับการเก็บรักษาไว้ในโถแก้ว ซึ่งข้างๆ กันนั้นเป็นปั๊มที่ใช้สำหรับฉีดสารซักฟอกเข้าไปในเส้นเลือดใหญ่ของหัวใจ (aorta) การไหลของสารเข้ามาทางนี้ทำให้ลิ้นปิดหลอดเลือดปิด แล้วสารซักฟอกก็ไหลเข้าสู่เครือข่ายของเส้นเลือดฝอยที่ไปหล่อเลี้ยงกล้ามเนื้อหัวใจทั้งหมด โดยการฉีดสารซักฟอกนี้ได้ทำอยู่เป็นเวลาหลายวันจนกว่าเซลล์เดิมของเจ้าของจะตายและถูกกำจัดออกไปแล้วทั้งหมด Ott กล่าวว่า การไหลเข้าไปของสารซักฟอก จะเข้าไปกำจัดไขมัน DNA โปรตีนที่ละลายน้ำได้ น้ำตาล และสารเกือบทุกชนิดของเซลล์ออกมา เหลือไว้เพียงแค่โครงสร้างตาข่ายของคอลลาเจนสีซีดๆ ลามินินส์ (laminins) และโปรตีนโครงสร้าง (หรือที่เรารู้จักกันว่า extracellular matrix ที่ใช้สำหรับเชื่อมหัวใจทั้งหัวใจให้คงตัวอยู่ได้)
การผลิตโครงสร้างของหัวใจนี้ไม่จำเป็นว่าจะต้องใช้หัวใจมนุษย์เท่านั้น หัวใจของหมูก็เป็นความหวังถัดไปของการศึกษา เนื่องจากหัวใจหมูมีองค์ประกอบของสารที่อยู่ภายนอกเซลล์ ที่สำคัญแบบเดียวกับของหัวใจมนุษย์ และหัวใจหมูก็ไม่เป็นพาหะนำโรคของมนุษย์ อีกอย่างก็คือหัวใจของหมูจะไม่มีอ่อนแอจากความไม่สบาย หรือเสียหายจากความพยายามในการยื้อชีวิต เหมือนกับหัวใจของมนุษย์ “เนื้อเยื่อของหมูปลอดภัยกว่าเนื้อเยื่อของมนุษย์มาก และที่สำคัญที่สุดเราสามารถหามันมาได้อย่างไม่จำกัดเลย” Stephen Badylak นักวิจัยด้านเวศศาสตร์ฟื้นฟู แห่งมหาวิทยาลัยพิตส์เบิร์ก กล่าว
Ott กล่าวเสริมว่า ส่วนที่ยากที่สุดก็คือ เราจะต้องมั่นใจว่า สารซักฟอกที่ฉีดเข้าไปในหัวใจนี้มันไปละลายสารต่างๆ ในหัวใจในปริมาณที่เหมาะสม ถ้าเรากำจัดสารต่างๆ ในหัวใจมากเกินไป หัวใจอาจจะยังมีโมเลกุลต่างๆ จากผนังเซลล์เดิมที่จะนำไปสู่การปฏิเสธอวัยวะจากระบบภูมิคุ้มกันของผู้รับก็ได้ แต่ถ้าเรากำจัดสารต่างๆ ของหัวใจมากเกินไป มันอาจจะทำให้สูญเสียโปรตีนที่สำคัญๆ และสารที่ส่งผลต่อการเจริญเติบโต (growth factors) ที่มีผลต่อเซลล์ใหม่ที่เราจะนำเข้ามาปลูกในหัวใจนี้ โดยสารเหล่านี้เองจะเป็นตัวบ่งบอกว่าเซลล์แต่ละเซลล์ว่าจะต้องเรียงตัว และมีพฤติกรรมเช่นใด “ถ้าเราใช้สารซักฟอกที่อ่อนๆ และใช้เวลาสั้นๆ เราจะได้ผลลัพธ์ที่ดีขึ้น” Thomas Gilbert กล่าว
จากการลองผิดลองถูกหลายร้อยครั้ง โดนการค่อยๆ ปรับความเข้มข้น เวลา และความดันของสารซักล้างที่ฉีดเข้าไปในหัวใจ นักวิจัยก็เริ่มเห็นผลลัพธ์ของกระบวนการกำจัดเซลล์หัวใจที่ดียิ่งขึ้นไปเรื่อยๆ และนี่น่าจะเป็นช่วงที่ดีที่สุดที่ดีที่สุดของการพัฒนาการสร้างอวัยวะประดิษฐ์ แต่ว่ามันยังเป็นเพียงแค่จุดเริ่มต้น ซึ่งบันไดขั้นถัดไป ก็คือ โครงสร้างที่ผลิตได้นี้จำเป็นจะต้องเอาเซลล์ของมนุษย์เข้าไปปลูกถ่าย
เซลล์
การถ่ายเซลล์ (Recellularization) ก็เป็นความท้าทายที่ยิ่งใหญ่อีกประการหนึ่ง Jason Wetherim ศัลยแพทย์กล่าว “ปัญหาก็คือ เราจะใช้เซลล์อะไร เท่าไร และจะใช้เซลล์ที่โตเต็มที่สมบูรณ์แล้ว หรือสเต็มเซลล์จากเอ็มบริโอ หรือสเต็มเซลล์ที่ได้รับการเหนี่ยวนำให้เกิด (induced pluripotent stem cells) และเราจะเอาเซลล์พวกนั้นมาจากแหล่งไหน”
“อันที่จริง คุณไม่สามารถเอาเซลล์หัวใจของผู้ใหญ่มาเพิ่มจำนวนต่อไปได้อีกนะ” เทเลอร์กล่าว “ถ้าคุณสามารถทำได้ เราก็ไม่จำเป็นจะต้องคุยกันเรื่องนี้หรอก” เพราะว่าถ้าเป็นแบบนั้นจริงเซลล์หัวใจที่เสียหายไปแล้ว มันก็จะซ่อมแซมตัวมันเองได้ และก็ไม่จำเป็นที่จะต้องผ่าตัดเปลี่ยนถ่ายอวัยวะหรอก
นักวิจัยในสาขานี้ส่วนใหญ่ มักจะใช่ส่วนผสมของเซลล์สองประเภท หรือมากกว่านั้น อาทิ ใช้เซลล์ต้นกำเนิดของเซลล์พื้นผิว เพื่อเอามาเรียงตัวตามผนังหลอดเลือด และเซลล์ต้นกำเนิดกล้ามเนื้อ สำหรับสร้างผนังและห้องต่างๆ ของหัวใจ โดย Ott นำเซลล์เหล่านี้มาจาก สเต็มเซลล์ประเภทที่เหนี่ยวนำให้เกิด กล่าวคือ เป็นเซลล์ของผู้ใหญ่ ที่ถูกเปลี่ยนโปรแกรมใหม่ให้กลับไปเป็นเซลล์เสมือนกับอยู่ในสถานะของสเต็มเซลล์ของเอ็มบริโอ โดยการใช้ growth factors เป็นตัวกระตุ้น ซึ่งสเต็มเซลล์ประเภทนี้ เราสามารถนำออกมาจากตัวผู้ป่วยที่ต้องการปลูกถ่ายอวัยวะเอง และข้อดีอีกอย่างก็คือเนื้อเยื่อใหม่ที่สร้างได้ก็จะไม่ถูกปฏิเสธจากผู้ป่วยอย่างแน่นอน
โดยหลักการแล้ว วิธีการใช้สเต็มเซลล์ชนิดเหนี่ยวนำนี้ จะทำได้หัวใจใหม่มีเซลล์หัวใจครบทุกประเภท ซึ่งประกอบไปด้วย เซลล์เส้นเลือด และเซลล์กล้ามเนื้อหัวใจทุกแบบ แต่ในทางปฏิบัติแล้ว วิธีแบบนี้ก็มีปัญหาของมันเอง คือขนาดของหัวใจ โดยจำนวนเซลล์ที่ได้มันต่ำกว่าที่เราพึงพอใจ Ott กล่าวเสริมว่า “เราต้องการเซลล์ชนิดหนึ่งเพียงแค่ 1 ล้านเซลล์ ในขณะที่เซลล์อีกชนิดหนึ่งเราต้องการถึง 100 ล้าน หรือ 50,000 ล้านเซลล์” และนักวิจัยก็ยังไม่ทราบว่า สเต็มเซลล์ชนิดที่ถูกเหนี่ยวนำนี้ มีพัฒนาไปเป็นเซลล์หัวใจที่ถูกชนิดหรือเปล่า

เมื่อเซลล์ต่างๆ เริ่มเจริญเติบโตบนโครงสร้างของหัวใจ เซลล์ที่ยังไม่เจริญเติบโตเต็มที่บางเซลล์เริ่มวางราฐานบนโครงสร้างนั้นๆ และเริ่มโตขึ้น แต่ว่าการกระตุ้นให้มันทำงานได้ หรือเป็นเซลล์หัวใจที่สมบูรณ์แบบและเต้นได้นั้น ความต้องการมากว่าแค่ออกซิเจนและสารที่ส่งผลต่อการเจริญเติบโตเท่านั้น “เซลล์ทุกเซลล์รับรู้ว่ามีอะไรบ้างที่อยู่รอบๆ ตัวมัน” Angela Panoskaltsis-Mortari นักวิจัยที่พยายามจะสร้างปอดสำหรับการเปลี่ยนถ่ายกล่าว “เซลล์ไม่เพียงแค่รับสัญญาณจาก growth factors เท่านั้น มันยังรับรู้ถึงความเมื่อยล้า และแรงกดดันต่างๆ จากสิ่งแวดล้อมรอบๆ อีกด้วย” ซึ่งองค์ประกอบทั้งหมดทั้งมวลนี้ เป็นตัวควบคุมว่าเซลล์แต่ละเซลล์ จะมีการพัฒนาต่อไปในทิศทางใด
ดังนั้น นักวิจัยได้นำหัวใจไปไว้ในเครื่องปฏิกรณ์ชีวภาพ (bioreactor) ซึ่งเลียนแบบระบบความรู้สึกและการเต้นของหัวใจ โดยเครื่องปฏิกรณ์ชีวภาพที่ Ott ใช้นี้ เขาใด้ใส่องค์ประกอบของสัญญาณไฟฟ้า ที่เหมือนกับสัญญาณจังหวะการเต้นของหัวใจเข้าไปด้วย เพื่อช่วยให้เซลล์กล้ามเนื้อหัวใจทั้งหมดสามารถเต้นประสารกันได้ กอปรกับจังหวะการเต้นทางกายภาพที่ถูกกำหนดด้วยปั๊ม แต่อย่างไรก็ตามนักวิจัยยังคงเผชิญหน้ากับความพยายามที่จะเลียนแบบสภาวะที่แท้จริงของร่างกาย อย่างเช่น การเปลี่ยนแปลงจังหวะการเต้นของหัวใจ ความดันโลหิต หรือแม้กระทั้งการใช้ยาที่ส่งผลต่อการเต้นหัวใจในผู้ป่วย “ร่างกายของมนุษย์ตอบสนองต่อสิ่งเร้ารอบๆ ข้างอย่างรวดเร็ว ซึ่งมันแทบจะเป็นไปไม่ได้เลยที่จะสร้างเครื่องปฏิกรณ์ชีวภาพที่สามารถเลียนแบบสภาวะแบบนั้นได้ทั้งหมด” Badylak กล่าว
เทเลอร์ และ Ott ได้พัฒนาเครื่องปฏิกรณ์ชีวภาพเป็นครั้งแรก เพื่อเลี้ยงเซลล์หัวใจของหนูก่อน “ในห้องแลบของเรามีเทปกาวติดอยู่ในแลยเยอะมาก” Ott กล่าว แต่ในที่สุดแล้ว หัวใจประดิษฐ์ ก็ค่อยๆ เริ่มที่จะเต้นเองได้ ภายหลังที่อยู่ในเครื่องปฏิกรณ์ชีวภาพเป็นเวลา 8 – 10 วัน โดยที่หัวใจประดิษฐ์นี้ มีความสามารถในการปั๊มเลือดอยู่เพียงแค่ 2% ของความสามารถของหัวใจของหนูปกติ [1] เทเลอร์กล่าวเสริมต่อไปอีกว่า ตอนนี้เธอสามารถทำให้หัวใจของหนู และสัตว์เลี้ยงลูกด้วยนมที่มีขนาดใหญ่ขึ้น มีความสามารถในการปั๊มเลือดอยู่ที่ประมาณ 25% ของสภาวะปกติแล้ว โดยที่เขาทั้งสองต่างก็มั่นใจว่า ทางที่เขาเลือกเดินนั้นถูกต้องแล้ว
จังหวะหัวใจ
ความท้าทายสิ่งสุดท้าย ซึ่งนับว่าเป็นสิ่งที่ยากที่สุดก็คือ การเอาหัวใจประดิษฐ์ที่เพิ่งจะเพาะเลี้ยงออกมาได้ ใส่เข้าไปในสิ่งมีชีวิตอีกครั้งหนึ่ง และทำให้มันสามารถเต้นต่อไปได้
ความสมบูรณ์ของระบบหลอดเลือดทั้งหมด เป็นปราการด่านแรก ทุกๆ ส่วนของสารระหว่างเซลล์เปลือยๆ เป็นชนวนที่จะทำให้เลือดแข็งตัวและอุดตันได้เสมอ ซึ่งมันจะเป็นอันตรายถึงชีวิตแก่สัตว์ “คุณต้องการเซลล์ผนังหลอดเลือดทั้งหมดที่สมบูรณ์ที่สุด ไม่อย่างนั้นแล้ว เลือดก็จะแข็งตัวและอุดตันหลอดเลือดหรือไม่ก็รั่วออกมาได้” Gilbert กล่าว
Ott แสดงให้ดูว่า อวัยวะประดิษฐ์ชิ้นใหม่ของเขาสามารถมีชีวิตรอดได้ โดยครั้งแรก กลุ่มของเขาได้ผ่าตัดเปลี่ยนถ่ายปอดข้างหนึ่งให้กับหนู และความสามารถในการแลกเปลี่ยนแก๊สทีเกิดขึ้นในปอดใหม่นี้เกิดขึ้นได้ดี แต่ทว่าสุดท้ายก็มีของเหลวมาเติมช่องอากาศในปอดอย่างรวดเร็ว [4] และการผ่าตัดเปลี่ยนถ่ายไตประดิษฐ์ของเขาในหนูก็ได้ผลเป็นที่น่าพึงพอใจ แต่ว่าไตประดิษฐ์นั้นสามารถกรองปัสสาวะได้น้อยเกินไป ซึ่งอาจจะเป็นเพราะว่าจากกระบวนการปลูกถ่ายเซลล์ในไตนั้นได้ใช้ประเภทของเซลล์น้อยเกินไปก็ได้ [5] เขาและทีมของเขายังคงผ่าตัดปลูกถ่ายหัวใจให้กับหนูไปแล้วอีกด้วย โดยเอาหัวใจใหม่ไว้ตรงคอ หรือไม่ก็ในท้อง ข้างๆ กับหัวใจเดิม แต่ว่า นักวิจัยก็พบปัญหาที่ว่า เขาสามารถทำให้หัวใจใหม่นี้ เต้นอยู่ได้เพียงแต่ช่วงเวลาหนึ่งเท่านั้น และไม่มีหัวใจชิ้นไหนเลยที่มีความสามารถในการปั๊มเลือดได้จริงๆ โดยในที่สุดแล้ว นักวิจัยจะต้องแสดงให้เห็นว่า หัวใจที่เขาประดิษฐ์กันขึ้นมานั้น ต้องมีความสามารถที่ดีขึ้นมากกว่านี้ก่อน ถึงจะสามารถทดลองในสัตว์ที่ใหญ่ขึ้นไปได้
Badylak กล่าวว่า “คุณต้องเริ่มต้นด้วยหัวใจที่สามารถทำงานได้ดีมากๆ” ก่อนที่จะนำไปผ่าตัดปลูกถ่ายเข้าไปในสิ่งมีชีวิต “คุณไม่สามารถเริ่มต้นจากหัวใจที่สามารถปั๊มได้เพียงแค่ 1% 2% หรือ 5% แล้วหวังว่าจะได้เห็นผลลัพธ์ที่แตกต่างหรอก” เขากล่าวโดยอ้างถึงความสามารถในการปั๊มน้ำเลือดของหัวใจ และเรื่องแบบนี้ ก็มีที่ว่างสำหรับความผิดพลาดเพียงแค่เล็กน้อยเท่านั้น “ตอนนี้เรายังอยู่ในช่วงเหมือนเด็กที่กำลังหัดเดินอยู่” Panoskaltsis-Mortari กล่าว “เราอยู่กับคนผ่าตัดเปลี่ยนถ่ายหัวไปแล้วมากว่าทศวรรศแล้ว”
กระบวนการเปลี่ยนเซลล์ใหม่ทั้งหมดนี้ ตอนนี้ได้ถูกใช้สำหรับในการพัฒนาลิ้นหัวใจ และส่วนอื่นๆ ของให้ใจให้ดียิ่งขึ้น ยกตัวอย่าง ลิ้นหัวใจที่ประดิษฐ์โดยวิธีนี้ มีอายุยืนยาวว่าลิ้นหัวใจเทียม หรือลิ้นหัวใจที่ได้จากผู้เสียชีวิตโดยตรง และที่สำคัญที่สุด ลิ้นหัวใจแบบนี้ มีศักยภาพที่จะโตขึ้นไปพร้อมๆ กับผู้ป่วย และถ้ามันเสียหายไป มันก็ยังสามารถที่จะซ่อมแซมตัวของมันเองได้อีกด้วย และอวัยวะบางอวัยวะนั้น ไม่จำเป็นที่จะต้องผ่าตัดเปลี่ยนถ่ายทั้งหมด “ฉันต้องแปลกในแน่ๆ ว่าในอีก 5 ถึง 7 ปีข้างหน้า ฉันไม่เห็นคนไข้ที่ผ่าตัดปลูกถ่ายอวัยวะประดิษฐ์แบบนี้ อย่างน้อยก็ต้องเป็นบางส่วนของเส้นเลือด บางพูของปอด หรือส่วนหนึ่งตับ” Badylak กล่าว
เทเลอร์คาดว่า ส่วนหนึ่งของวิธีการแบบนี้ จะสามารถช่วยให้ผู้ป่วยจากความผิดปกติของหัวใจเพียงบางส่วนเท่านั้น อย่างเช่น สภาวะขาดความยืดหยุ่นของหัวใจซีกซ้าย โดยเป็นผลมาจากพัฒนาการที่ผิดปกติ การเปลี่ยนหัวใจแค่ครึ่งเดียว “มันเป็นแรงผลักดันที่สำคัญให้ร่างกายผลิตสิ่งต่างๆ ที่เราต้องการได้เอง” เธอกล่าว และจากความพยายามเหล่านี้ นักวิจัยก็ได้เรียนรู้ อย่างน้อยก็ที่ว่า เซลล์หัวใจมีการพัฒนาได้อย่างไร และการทำงานของเซลล์เหล่านี้ในแบบสามมิติ ในอนาคต ส่วนหนึ่งของโครงสร้าง ไม่ว่าจะมาจะการสังเคราะห์หรือซากศพ จะสามารถให้เซลล์ใหม่ๆ เข้ามาอาศัยอยู่แทนที่ได้ โดยเฉพาะส่วนที่เสียหายของหัวใจ และเซลล์ใหม่เหล่านั้น ก็จะซ่อมแซมตัวของมันเอง
อ้างอิง:
[1] Ott, H. C. et al. Nature Med. 14, 213–221 (2008).
[2] Zopf, D. A., Hollister, S. J., Nelson, M. E., Ohye, R. G. & Green, G. E. N. Engl. J. Med. 368, 2043–2045 (2013).
[3] Atala, A., Bauer, S. B., Soker, S., Yoo, J. J. & Retik, A. B. Lancet 367, 1241–1246 (2006).
[4] Ott, H. C. et al. Nature Med. 16, 927–933 (2010).
[5] Song, J. J. et al. Nature Med. 19, 646–651 (2013).
ที่มา: https://www.nature.com/news/tissue-engineering-how-to-build-a-heart-1.13327






29 สิงหาคม 2014 2:43
เป็นบทความที่ดีมากครับ ถึงแม้ผมยังอาจไม่จบ ก็ได้แรงกระตุ้นอะไรหลายๆอย่าง ในเรื่องความคิดของมนุษย์ไร้ขอบเขตจริงๆครับ ในไทยงานวิจัยแนวนี้จะมีมั้ยครับ ถ้ามีแนะนำ จะขอบคุณมากครับ ^^